پژوهشگران
با استفاده از نور و نانوذرات رودیوم، راهی برای تبدیل دیاکسید کربن به
جزء سازندهی بسیاری از سوختها یافتهاند. این واکنش شیمیایی تازه
کشفشده، میتواند از نور طبیعی خورشید برای کاهش سطوح دیاکسید کربن در جو
استفاده کند و به توسعهی انرژیهای جایگزین بدون ایجاد محصولات جانبی
مانند مونوکسید کربن منجر شود.
نور
فرابنفش این واکنش را به پیش میراند. این امر با استفاده از نانوذرات
رودیوم در ارتباط با پلاتین رخ میدهد. استفاده از نور به جای گرما نهتنها
بهینهتر است، بلکه تولید متان نسبت به سایر محصولات جانبی مزاحم را
افزایش میدهد.
این خبر برای صنعت فضایی جالب خواهد بود؛ چرا که متان یکی از سوختهای مدنظر برای سفر به مریخ است.
وقتی
نور را به نانوساختارهای رودیوم میتابانیم، میتوانیم جهت واکنش شیمیایی
را تعیین کنیم (واکنش در جهت رفت پیشرفت کند یا برگشت). بنابراین باید
بررسی میکردیم که وقتی نمی توانیم از حرارت استفاده کنیم، چگونه با نور
جهت واکنش را انتخاب کنیم.
ماده
ای پودری تشکیلشده از نانومکعبهای رودیوم سنتزشده در محفظه واکنش قرار
گرفت و سپس مخلوط دیاکسید کربن و هیدروژن از آن عبور داده شد. وقتی که به
نانوذرات با الایدی فرابنفش پرقدرت نور تابانده شد، واکنش در دمای اتاق
انجام شد و مقدار بسیار زیادی متان تولید کرد. این واکنش اگر بخواهد تحت
حرارت انجام شود، نیاز به دمایی نزدیک به ۳۰۰ درجهی سانتیگراد خواهد داشت
و مقدار زیادی مونوکسید کربن نیز تولید خواهد کرد. اختلاف بین این دو روش،
قابل توجه است.
دانشمندان معتقدند که توانایی کنترل خروجی یک واکنش بهعنوان گزینش پذیری آن، در این واکنش مشهود است.
هزینههای
واکنشی که فقط ۵۰ درصد گزینش پذیر است، نسبت به واکنشی که ۱۰۰ درصد گزینش
پذیر است، دو برابر خواهد بود. اگر گزینش پذیری واکنش خیلی بالا باشد، شما
نیازی به خالصسازی محصول نخواهید داشت و در زمان و انرژی صرفهجویی خواهد
شد.
این
پیشرفت در زمینهی پلاسمونیکها صورت گرفته است و شامل استفاده از نور
برای انرژی دادن به ذرات ریز فلز در مقیاس نانو است. تاکنون این رویکرد در
سلولهای خورشیدی جدید و ذخیرهی دیتا، نتیجه بخش بوده است. رودیوم گرچه
نایاب است، اما مقدارهای کم آن در حال حاضر به عنوان کاتالیزور در سرعت
بخشی به فرایندهای صنعتی مانند تولید کودهای شیمیایی، مواد شوینده و مواد
دارویی استفاده میشود. به همین دلیل برای این آزمایشها نیز انتخاب شد.
این ماده میتواند در مبدلهای کاتالیزوری سیستم اگزوز ماشینها نیز یافت
شود.
نانوذرات
فلزی پلاسمونیک به عنوان آنتنهای کوچک عمل میکنند که میتوانند نور مرئی
یا فرابنفش را با بازده بالایی جذب و میدانهای قوی الکتریکی ایجاد کنند.
در چندین سال اخیر، این بحث مطرح بوده که این ویژگی ممکن است به عنوان
خاصیت کاتالیزوری اطلاق شود.
در
قدمهای بعدی، پژوهشگران بررسی خواهند کرد که آیا نور میتواند دیگر
واکنشهایی که رودیوم حرارت دیده به عنوان کاتالیست در آنها عمل میکند،
بهبود بخشد یا خیر. علاوه بر این، آنها امید دارند که نتایج این پژوهش را
در عمل به کار ببندند. اگر این واکنش با نور خورشید نیز انجام شود، آن گاه
این واکنش میتواند به جزئی از سیستمهای انرژی تجدید پذیر اضافه شود.
مقالهی مربوط به این واکنش در Nature Communications منتشر شده است.
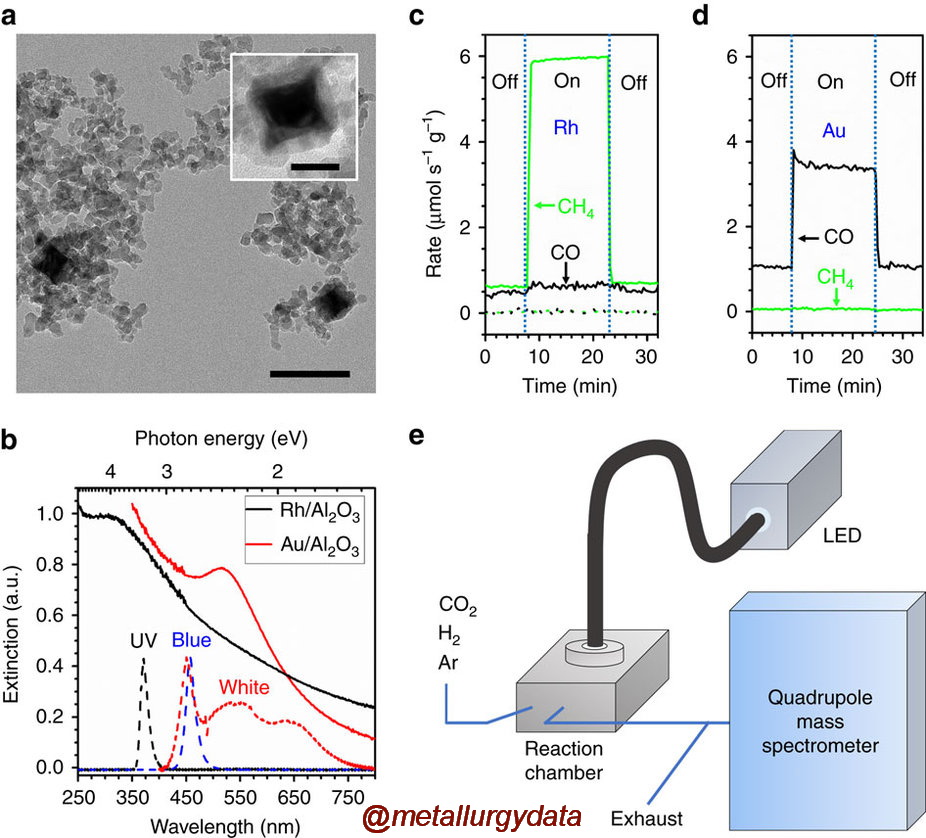
(a) TEM images of the Rh/Al2O3 photocatalyst. Scale bar, 100 nm (inset: 25 nm). (b) Ultraviolet–visible extinction spectra (solid lines) of the Rh/Al2O3 (black) and Au/Al2O3 (red) photocatalysts, measured by diffuse reflectance in an integrating sphere, overlaid with the emission spectra (dotted lines) of the ultraviolet (black), blue (blue) and white (red) LEDs. (c) Rates of CH4 (green) and CO (black) production at 623 K on Rh/Al2O3 (solid lines) and Al2O3 (dotted lines) under dark and ultraviolet illumination at 3 W cm−2. CH4 production is strongly and selectively enhanced by ultraviolet light on the Rh photocatalyst. Neither CH4 nor CO production was detected on Al2O3. (d) Rates of CO (black) and CH4 (green) production at 623 K on Au/Al2O3 under dark and white light illumination at 3 W cm−2. A light-enhanced reaction rate is observed, but CO remains the exclusive product under both conditions. (e) Schematic of the photocatalytic reaction system, consisting of a stainless steel reaction chamber with a quartz window, LEDs coupled through a light guide, and a mass spectrometer for product analysis.
